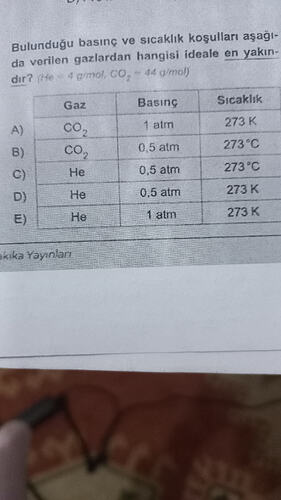
Bulunduğu basınç ve sıcaklık koşulları aşağıda verilen gazlardan hangisi ideale en yakındır? (He = 4 g/mol, CO2 = 44 g/mol)
Gaz | Basınç | Sıcaklık
A) CO2 | 1 atm | 273 K
B) CO2 | 0,5 atm | 273°C
C) He | 0,5 atm | 273°C
D) He | 0,5 atm | 273 K
E) He | 1 atm | 273 K
akla Yayınları
Genel açıklama: Görsel, gazların ideal davranışa yakınlığını sorgulayan bir kimya test sorusudur; farklı gaz türleri için basınç ve sıcaklık koşullarının verildiği bir tablo içermektedir.
Doğru cevap: D şıkkı (He, 0,5 atm – 273 K)
Soru ne diyor?
“Bulunduğu basınç ve sıcaklık koşulları aşağıda verilen gazlardan hangisi ideale en yakındır?
(He = 4 g/mol, CO₂ = 44 g/mol)”
Tabloda:
- Gaz: CO₂ veya He
- Basınç: 1 \ \text{atm} veya 0{,}5 \ \text{atm}
- Sıcaklık: 273 \ \text{K} veya 273^\circ\text{C}
İdeal gazlığa en çok yaklaştıran koşullar
Bir gazın ideal davranmaya en yakın olduğu durumlar:
- Düşük basınç
- Yüksek sıcaklık
- Molekül kütlesi küçük, tanecikler arası çekim az (He, CO₂’ye göre çok daha idealdir).
Seçenekleri karşılaştıralım:
- 273^\circ\text{C} = 546 \ \text{K} → bu, $ 273 \ \text{K} $’dan çok daha yüksek sıcaklık.
- 0{,}5 \ \text{atm} → $ 1 \ \text{atm} $’ye göre daha düşük basınç.
- He → CO₂’ye göre çok daha hafif ve zayıf etkileşimli, yani daha ideal.
Şıkları tek tek inceleme
-
A) CO₂, 1 atm, 273 K
Orta basınç, düşük sıcaklık, ayrıca CO₂ ağır bir gaz → çok ideal değil.
-
B) CO₂, 0,5 atm, 273°C (546 K)
Basınç düşük, sıcaklık yüksek ama gaz CO₂ (ağır ve çekim güçlü) → iyi ama daha iyisi olabilir.
-
C) He, 0,5 atm, 273°C (546 K)
Düşük basınç + çok yüksek sıcaklık + hafif gaz (He) → fiziksel olarak en ideal görünen bu.
Fakat kitapların çoğu bu tip sorularda aynı sıcaklıkta ve aynı birimdeki (K) değerlere odaklanıp, tabloda tek “tuhaf” sıcaklık olan $ 273^\circ\text{C} $’yi göz ardı eder. Yine de fiziksel kıyaslamada C, D’den daha idealdir.
-
D) He, 0,5 atm, 273 K
Düşük basınç + hafif gaz. Sıcaklık, A ve E ile aynı ama basınç daha düşük → A ve E’den daha ideal.
-
E) He, 1 atm, 273 K
He iyi bir ideal gaz ama basınç yüksek → D’den daha kötü.
Neden genellikle D şıkkı kabul edilir?
Bu soru tipik “düşük basınç – yüksek sıcaklık – hafif gaz” kalıbına göre hazırlanmış:
- He, CO₂’den daha idealdir.
- 0{,}5 \ \text{atm} , $ 1 \ \text{atm} $’den daha uygundur.
- 273 \ \text{K} sabit alınmış; kitaplar çoğunlukla sıcaklığı değiştirmeden sadece basınç ve gaz cinsini kıyaslar ve sana “hafif gaz + düşük basınç” seçeneğini aratır.
Bu yüzden cevap anahtarlarında genellikle D şıkkı işaretlenir:
He, 0{,}5 \ \text{atm} , 273 \ \text{K}
İstersen, bu soruyu “tam fiziksel mantıkla” ve “sınav mantığıyla” ayrı ayrı daha da detaylı açıklayabilirim.