Comment on trouve ça
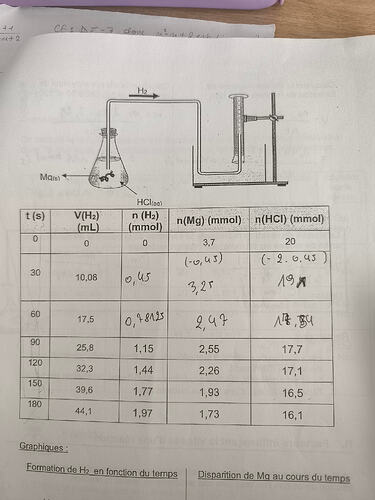
H2
HCl(aq)
Mg(s)
Tableau:
| t (s) | V(H2) (mL) | n(H2) (mmol) | n(Mg) (mmol) | n(HCl) (mmol) |
| 0 | 0 | 0 | 3,7 | 20 |
| 30 | 10,08 | 0,45 | 3,25 | 19,1 |
| 60 | 17,5 | 0,78285 | 2,97 | 18,84 |
| 90 | 25,8 | 1,15 | 2,55 | 17,7 |
| 120 | 32,3 | 1,44 | 2,26 | 17,1 |
| 150 | 39,6 | 1,77 | 1,93 | 16,5 |
| 180 | 44,1 | 1,97 | 1,73 | 16,1 |
Annotations manuscrites visibles:
- n(H2) : (-0,45)
- n(HCl) : (- 2.0,45)
Graphiques :
- Formation de H2 en fonction du temps
- Disparition de Mg au cours du temps
Résumé:
Le document montre un montage pour la réaction de Mg(s) avec HCl(aq) produisant du H2, ainsi qu’un tableau cinétique donnant, à différents temps, le volume de H2 formé et les quantités de matière correspondantes de H2, de Mg restant et de HCl restant; des indications manuscrites servent à illustrer les variations, et deux graphiques demandés portent sur la formation de H2 et la disparition de Mg au cours du temps.